t细胞是什么(细胞是图片)
CAR-T细胞治疗是目前血液肿瘤治疗领域冉冉升起的一颗新星,近年来发展迅速,给予了众多复发难治血液肿瘤患者新的希望。但与卓越的疗效相伴,CAR-T细胞治疗的安全性仍需长期数据评估,出凝血异常是其中常见的一种不良反应。
在2022年6月24日-26日召开的第七届上海国际淋巴肿瘤高峰论坛暨第三届国家血液转化和创新论坛上,华中科技大学同济医学院附属协和医院胡豫教授通过一例病例引入,对CAR-T细胞治疗中的出凝血异常从定义、致病机制、预防及治疗措施等方面进行了详尽讲解,并对即将公布的《嵌合抗原受体T细胞治疗相关出凝血功能障碍管理的中国专家共识》进行了框架梳理。
病例引入
患者,男,10岁。
2007年11月确诊急性B淋巴细胞白血病(Com-B,标危),按照CCLG08方案化疗2.5年,持续完全缓解。2014年3月,病情复发,再次行DVLD诱导化疗达完全缓解,续以CAM及HD-MTX巩固治疗2次。2015年11月,病情复发, 2015年12月3-7日给予DXM+Flu+Ara-C化疗。2015年1月12日,患者病情再次复发,纳入CD19特异性CAR-T细胞治疗B-ALL临床试验。
2016年1月26日,患者接受CAR-T细胞回输。患者于Day4出现乏力、肌痛及低热症状,Day5出现血象下降,血压偏低,肺部可闻及湿啰音,Day6出现凝血功能异常,转氨酶升高,肺CT示感染较前加重,Day8出现持续高热,SpO2下降,皮肤出现出血点,Day9出现持续高热,体温持续高于40℃,Day12患者于输注血小板后出现休克,血压升高,出现呕吐、间断抽搐及意识丧失,下肢肌力Ⅰ级,行头CT检查排除脑出血可能,Day14患者停止抽搐,肌力恢复至Ⅲ级,患者于Day16肌力恢复至Ⅳ级,肺部听诊未闻及啰音,CT示感染好转。
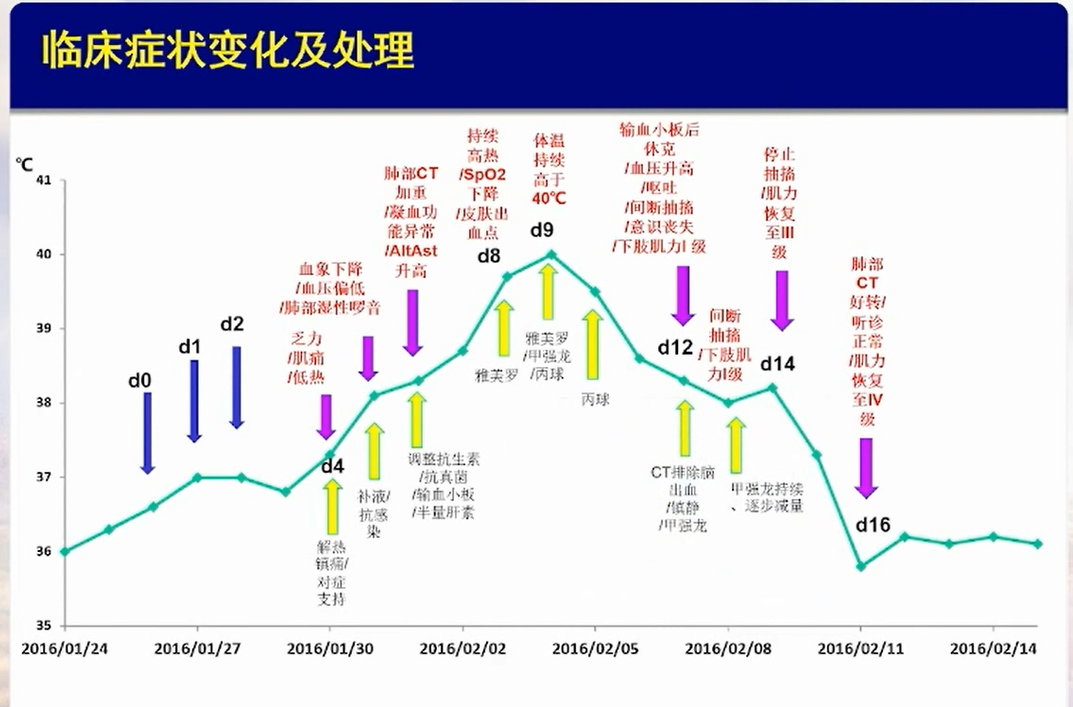
辅助检查结果提示:回输后,患者IL-6较正常值升高约72倍,IL-10较正常值升高约17倍。最终诊断为:CAR-T治疗后细胞释放综合征(CRS)合并巨噬细胞活化综合征、凝血功能异常、中枢神经系统异常、低免疫球蛋白血症及肺部感染。治疗上,在临床不同时期分别予以对症退热、抗感染、升压、补液、抗凝、输血及支持治疗,并予以白介素-6(IL-6)单抗、甲强龙等抗CRS治疗,相关症状得到控制,并于细胞回输后第21日达到细胞学完全缓解,MRD阴性。
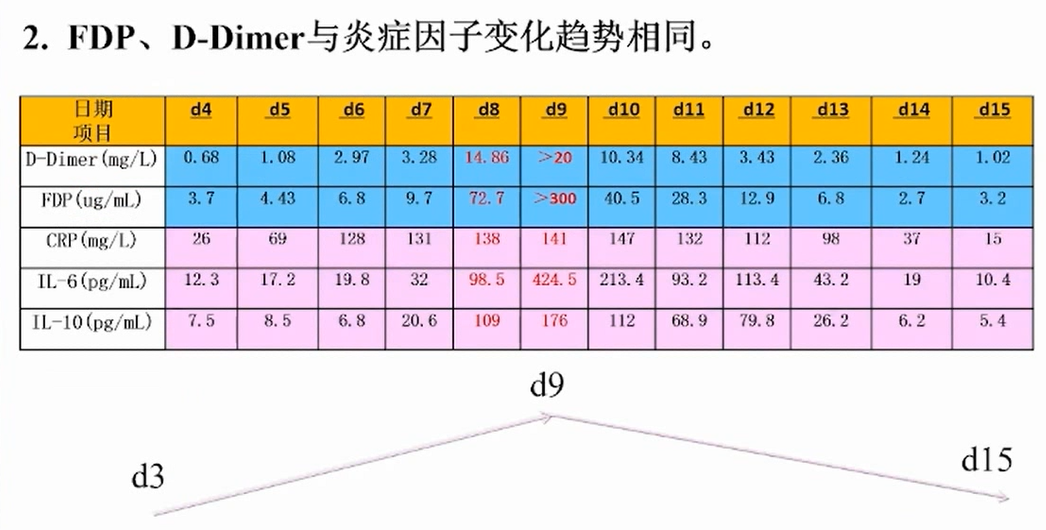
总结该病例凝血功能异常特点,可发现:凝血功能异常出现时间早,回输后第4天即出现凝血象改变,以活化部分凝血活酶时间(APTT)延长为主,纤维蛋白原降解产物(FDP)及D-二聚体(D-Dimer)明显升高,血小板动态下降,其中FDP及D-Dimer与炎症因子变化趋势相同。因此,考虑该患者凝血功能异常与CRS相关。
CRS与CRS相关出凝血功能障碍
CRS是CAR-T细胞治疗中一种常见且较为严重的不良反应,可波及体内原有的T细胞、B细胞、单核/巨噬细胞及树突状细胞等,引发细胞因子级联释放,介导体内多种免疫反应,继发低免疫球蛋白血症、巨噬细胞活化综合征、肝肾功能衰竭、肿瘤溶解综合征、弥散性血管内凝血(DIC)及神经系统改变等,从而产生临床症状。
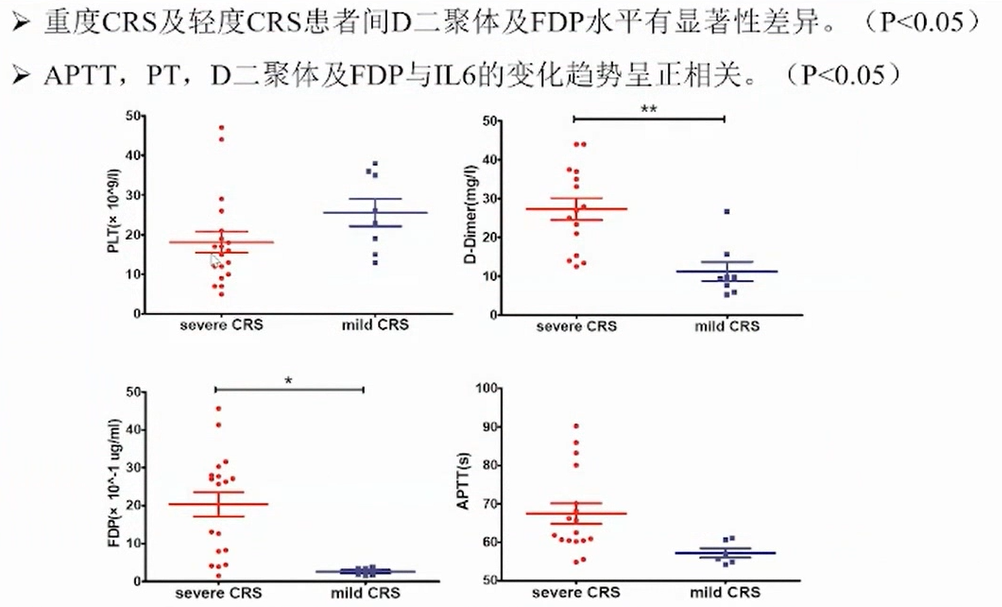
胡豫教授对中心内53例接受CAR-T细胞治疗的患者进行回顾性分析,30例发生出凝血功能障碍(56.6%),包括出血表现及实验室结果异常,表现为血小板下降,FDP明显升高,APTT显著延长,通常紧随IL-6升高而发生,在CRS得到控制后减轻。19例重度CRS患者均发生出凝血功能障碍,与此相对,34例轻度CRS患者中仅11例发生出凝血障碍。通过归纳病例特点,胡豫教授将此种CAR-T细胞治疗中的出凝血功能障碍定义为CRS相关出凝血功能障碍。
53例患者中,15例(28.3%)患者符合DIC诊断。对比之下重度CRS患者(14/19,73.7%)比轻度CRS患者(1/34,2.9%)更容易发生DIC,且CRS分级与CDSS积分成正相关。通过严格管控CRS及出凝血障碍,DIC及非DIC患者间生存率并无明显差异。
CRS相关出凝血功能障碍
发生机制
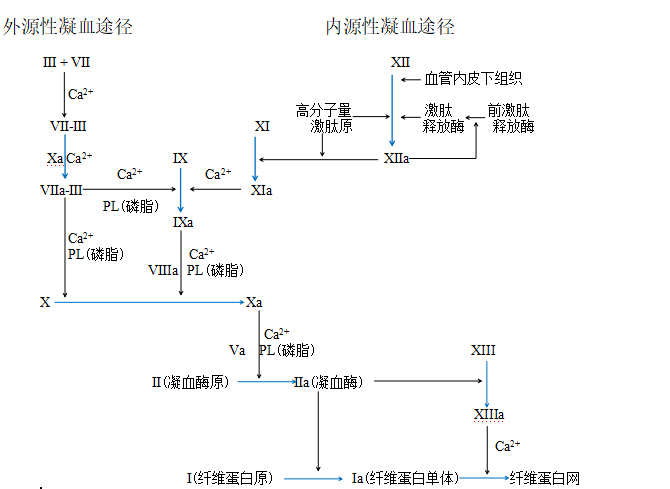
CRS可引发微血管体系损伤,肿瘤坏死因子α(TNF-α)、IL-1β及IL-6等细胞因子大量释放,可与凝血激活过程互相促进,通过抑制抗凝途径,消耗血小板及凝血因子,促成微小血栓及微循环障碍,进一步形成多器官衰竭。具体关键机制如下:
(1)IL-6:IL-6是细胞因子风暴中的核心元素,其可通过作用于骨髓促进巨核细胞成熟,并刺激肝脏产生促血小板生成素及纤维蛋白原,同时促进组织因子在单核细胞表面表达,通过多种途径共同引发凝血功能异常。
(2)内皮屏障:CAR-T细胞释放的细胞因子会引起内皮细胞功能异常,表现为组织因子(TF)和纤溶酶原抑制物Ⅰ(PAI-Ⅰ)过度表达凝血激活,同时抗凝血酶(AT)蛋白C(PC)系统、TFPI等抗凝蛋白下调或受到抑制。
(3)组织因子释放:细胞因子的释放可促进组织因子在内皮细胞上的表达并提高其活性,从而加重凝血障碍。
(4)凝血酶合成:高表达的TF可促进局部凝血酶的大量生成,除进一步反馈激活凝血系统以外,还可以与内皮细胞和炎症细胞的蛋白酶激活受体(PAR)相结合,移植血栓调节蛋白(TM)的表达,从而抑制蛋白C系统的激活。
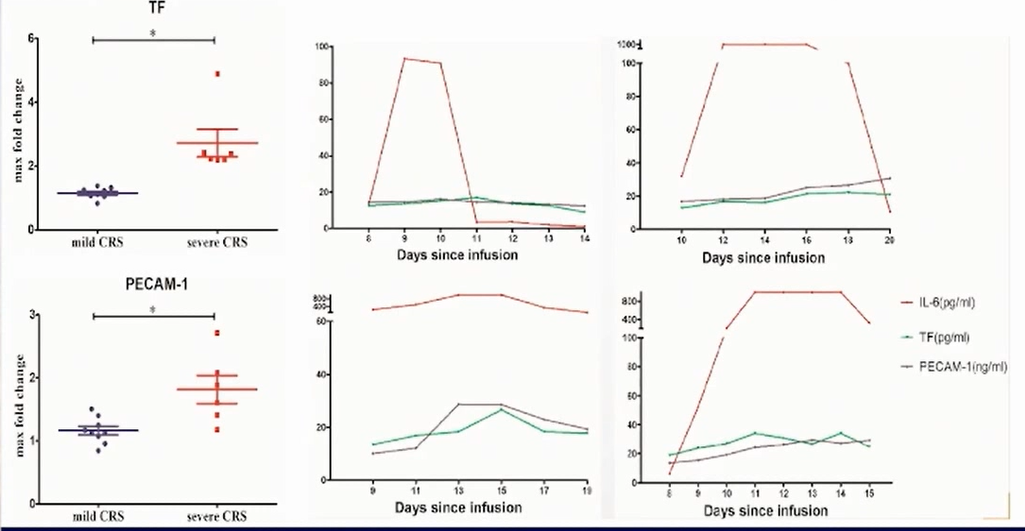
(5)血小板内皮细胞粘附分子(PECAM-1):胡豫教授团队发现,PECAM-1是血栓形成的负性调控分子,通过阻止血小板活化、抑制细胞因子产生及发挥作用、刺激血管产生前列腺素、构成内皮细胞间连接完整性等发挥其抗血栓作用。
通过检测15例患者的血浆TF及PECAM-1水平,发现二者在严重CRS患者中显著升高,并与IL-6浓度呈正相关。另外,不同等级CRS间,TF水平具有显著性差异,提示TF可作为CRS分级的一个重要参考指标。
(6)抗凝蛋白活性降低:多种抗凝蛋白合成减少,降解及消耗增多,且活性降低,从而引起凝血。AT对凝血酶及FXa、PC对FVa及FⅧa、TEPI对凝血酶生成的抑制能力均减弱,加重凝血障碍。其中,PC的含量与DIC发生风险呈现负相关性。
细胞免疫治疗
并发凝血功能障碍异常的处理
细胞免疫治疗中,CRS是出凝血障碍/DIC的重要诱因,其并发凝血功能异常多起病较急,病情进展迅速,严重者可威胁生命。控制关键在于控制细胞因子风暴,主要应注意以下几点:
(1)做好检测,早期发现:
FDP、D-Dimer、APTT、IL-6、IL-10、INF-γ及TNF-α应作为常规检测项目。细胞输注后CK增长倍数、净增长数值或增长率,以及铁蛋白与C反应蛋白(CRP)等亦对病情有提示意义,可视具体病情规律监测。
(2)鉴别诊断,排查诱因:
应与重度感染引发的出凝血异常(骨髓抑制状态易导致感染,可从热型、伴随症状、影像学检查及生化指标等方面进行鉴别)及肿瘤相关凝血异常(肿瘤溶解综合征及原发病复燃均可导致凝血异常,可通过疾病治疗阶段及疗效加以鉴别)相鉴别。
(3)合理评估分级,做好干预:
①I级:发热、恶心、呕吐、乏力、肌痛等非危及生命症状。干预措施:对症支持治疗;进行预防性感染评估。
②II级:脏器损害加重至2°,需氧量<40%。干预措施:如非老年无并发症同Ⅰ级,否则补液或单用低剂量升压药物,密切监测心脏及其他器官功能。
③III级:脏器损害加重至3°,需氧量>40%。干预措施:低剂量多重升压药物,抗IL-6治疗,酌情配合皮质激素治疗。
④IV级:脏器损害加重至4°,需呼吸机辅助支持。干预措施:中高剂量多重升压药物,抗IL-6治疗,酌情配合皮质激素治疗。
⑤V级:死亡。
(4)DIC的处理:
早期以抗凝为主,不宜单纯补充血小板和凝血因子,不宜抑制纤溶;中期在抗凝基础上补充血小板和凝血因子;晚期补充血小板和凝血因子,适量应用抗纤溶药物。

CAR-T相关出凝血功能障碍
治疗共识
中华医学会血液学分会血栓与止血学组联合中国研究型医院学会生物治疗学专业委员会即将于《中华血液学杂志》英文版刊登《嵌合抗原受体T细胞治疗相关出凝血功能障碍管理的中国专家共识》,对CAR-T相关出凝血功能障碍(CARAC)的理论与临床治疗要点进行了规范,主要要点如下:
(1)定义:CAR-T细胞回输后近期内(绝大多数在28天内),与细胞因子释放相关,患者发生出血和/或血栓并且伴随血小板下降及凝血指标异常的临床现象。病程可分为高凝期、出血期及脏器衰竭期。
(2)临床特征:
①出血:19.6%的CARAC患者发生有临床意义的出血,常为自发性,涉及皮肤、颌面部、消化道、呼吸道及颅内等多部位。
②血栓:在CAR-T治疗血液肿瘤中,血栓的发生率为6.3-8.8%,中位发生时间为治疗后第20-29天,包括肺栓塞、深静脉血栓、血栓性中风及内脏静脉血栓。
③DIC:约14-50%的出凝血功能障碍患者进展至DIC,相关临床表现包括瘀点/瘀斑、黄疸、低血压、呼吸困难、肾功能不全、神经系统异常、休克及严重出血等,其发生与CRS严重程度相关,而与患者年龄、性别及减淋巴细胞化疗方案等因素无关。
(3)诊断:
①Ⅰ级:CRS的存在及IL-6等细胞因子水平升高。
②Ⅱ级:血小板进行性下降、APTT及PT延长、INR升高、FIB降低、FDP及D-Dimer升高、TT延长及AT Ⅲ降低。
高肿瘤负荷患者、CAR-T细胞的高速扩增及高CRS级别是发生CARAC的高危因素。
若血小板<50×109/L或24小时内下降≥50%、D-Dimer≥5mg/L、PT延长≥3秒、APTT延长≥10秒、FIB<1.0g/L,应警惕DIC的发生。
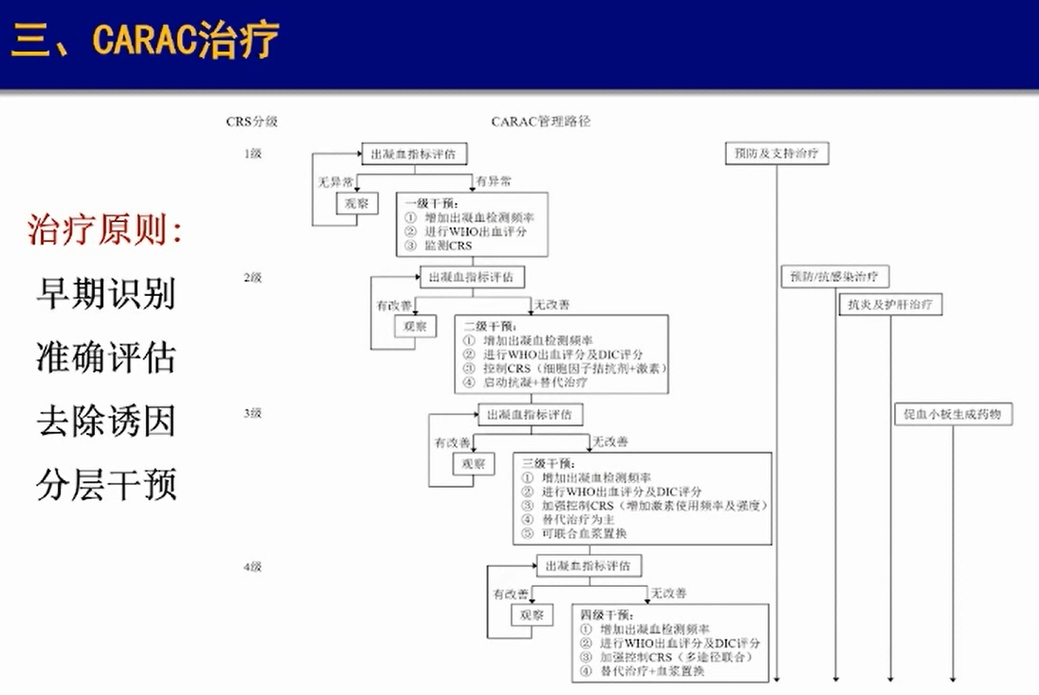
(4)治疗:
原则为:早期识别、准确评估、去除诱因、分层干预。
专家总结
出凝血异常是细胞治疗中的重要并发症之一,部分严重病例可出现DIC,细胞因子活化、内皮损伤、抗凝蛋白活性降低、粘附分子表达异常等可能与细胞免疫反应引起的出凝血异常相关,精确机制有待进一步探索。做好早期监测、采用DIC干预策略、分层分期治疗及控制CRS风暴是细胞免疫治疗并发出凝血异常防治的重点。

胡豫 教授
专家审阅:胡豫教授
荟萃名家,聚焦临床
欢迎关注CCMTV临床频道·血液科!






文章评论(0)